यहाँ हमने Class 12 Chemistry Chapter 10 Notes in Hindi दिये है। Class 12 Chemistry Chapter 10 Notes in Hindi आपको अध्याय को बेहतर ढंग से समझने में मदद करेंगे और आपकी परीक्षा की तैयारी में सहायक होंगे।
Class 12 Chemistry Chapter 10 Notes in Hindi
जैव अणु:- किसी जीव के शरीर में पाये जाने वाले वे जटिल कार्बनिक पदार्थ जो जीवन का मौलिक आधार होते हैं, जैव अणु कहलाते है।
या जैव रासायनिक क्रियाओ मे भाग लेने वाले जटिल अणुओ को जैव अणु कहते है।
उदा० – कार्बोहाइड्रेट्स, प्रोटीन, विटामिन लिपिड, एन्जाइम आदि ।
जैव अणुओ की जैव रासायनिक क्रिया से ऊर्जा प्राप्त होती है और यह ऊर्जा प्रत्येक सजीव की वृद्धि, मरम्मत, तथा सामान्य अभिक्रियाओ के लिए आवश्यक है।
कार्बोहाइड्रेट्स:- ये C , H व O युक्त पॉलीहाइड्रिक ऐल्डिहाइड या पॉलीहाइड्रिक कीटोन होते है।
- इनका सामान्य सूत्र Cx(H2O)y होता है।
- इनका सरलतम सूत्र [CH2O] होता है ।
- इनमे H व O का अनुपात सामान्यतः 2:1 होता है|
कार्बोहाइड्रेट्स के स्रोत: दूध , गन्ना, मक्का, केला, आम ,आलू, गाजर ,अंगूर जौ ,बाजरा, ज्वार आदि ।
- उदा०:- ग्लूकोज (रक्त शर्करा) → C6H12O6
- सुक्रोज (चीनी) → C12H22O11
- स्टार्च → (C6H10O5)n

कार्बोहाइड्रेट का वर्गीकरण –
(1) जल अपघटन के आधार पर:-
(a) मोनोसैकेराइड:- मोनोसैकेराइड में सामान्यतः तीन से सात तक कार्बन परमाणु होते हैं तथा इन्हें क्रमशः ट्रायोस (Trioses), टेट्रोस (Tettroses), पेन्टोस (Pentose), हैक्सोस (Hexose) तथा Heptose (हेप्टोस) कहते हैं।
उदा० –>

हैक्सोस के कुछ अन्य उदा० => ग्लूकोज, फ्रक्टोस तथा गैलेक्टोस
- प्रकृति में 20 प्रकार के मोनोसैकेराइड होते हैं।
- मोनोसैकेराइड को सरल शर्कराए भी कहा जाता है क्योंकि इनका जल अपघट नहीं होता है ।
(b) ओलिगो सैकेराइड:- इनका जल अपघटन होता है ।
- इनमें 2-10 कार्बन तक के यौगिक प्राप्त होता है।
- प्राप्त दो अणु मोनोसैकेराइड के समान या असमान हो सकते है।
- उदा० → माल्टोस, सूक्रोस व लैक्टोस
- Note ट्राई सेकेराइड उदा० → रेफिनोज
- टेट्रासैकेराइड उदा० → स्टेकीरोज
(c) पाली सेकेराइड:- इनका जल अपघटन होता है।
- पाली सेकेराइड में असंख्य मोनोसेकेराइड इकाईया ग्लाइकोसाइडी बन्ध द्वारा संयुक्त रहती है।
- यह प्रकृति में सर्वाधिक पाया जाने वाला कार्बोहाइड्रेट है। इसीलिए इन्हें जैव बहुलक या प्राकृतिक बहुलक कहते हैं ।
- ये अक्रिस्टलीय, स्वादहीन तथा जल में अविलेय है ।
उदा –> स्टार्च, सेलुलोस आदि ।
(2) स्वाद के आधार पर:-
(a) शर्कराएँ (Sugar):- शर्कराएं स्वाद में मीठी, जल में विलेय तथा क्रिस्टलीय ठोस होती है।
उदा० → ग्लूकोस, फ्रक्टोस, सुक्रोस, लैक्टोस, माल्टोस आदि।
(b) अशर्कराएँ (Non sugar):- अशर्करा स्वादहीन जल में अविलेय अथवा कोलॉयडी विलयन बनाने वाली अक्रिस्टलीय ठोस होती है।
उदा०→ स्टार्च, सेलुलोस, ग्लाइकोजन आदि ।
(3) अपचयन के आधार पर
(a) अपचायक शर्कराएं:- जो शर्कराएं अपचायक के रूप में प्रयुक्त होती है उन्हें अपचायक शर्करा कहते है।
उदा०→ ग्लूकोस, फ्रुक्टोज, लैक्टोस, माल्टोस आदि।
(b) अनअपचायक शर्कराएं:- ये टॉलेन अभिकर्मक तथा फेंहलिग विलयन का अपचयन नहीं करती है।
उदा० –>सुक्रोज
मोनोसैकराइड
ये प्रायः दो भागो में विभक्त होते हैं-
- (1) ऐल्डोस
- (2) कीटोस
ग्लूकोज
जैव जगत मे ग्लूकोज को सर्वाधिक महत्वपूर्ण मोनोसैकेराइड माना जाता है।
ग्लूकोज के भौतिक गुण:-
- (1) यह श्वेत रंग का क्रिस्टलीय ठोस है जिसका गलनांक1460C है।
- (2) यह जल में घुलनशील है।
- (3) यह ऐल्कोहॉल में अल्प विलेय है, परन्तु ईथर में अविलेय है।
- (4) यह प्रकाशिक सक्रिय यौगिक है तथा प्राकृतिक रूप से (+) ग्लूकोज अथवा डेक्स्ट्रो रूप में पाया जाता है।
- (5) यह परिवर्ती ध्रुवण घूर्णन दर्शाता है।
ग्लूकोज बनाने की विधियाँ : –
(1) सुक्रोज (चीनी) से:- सुक्रोज के जल अपघटन से ग्लूकोज तथा फ्रक्टोज का सम अणुक मिश्रण प्राप्त होता है।

ग्लूकोज तथा फ्रक्टोज को इनके मिश्रण से Ca (OH)2 के द्वारा पृथक कर लेते है ।
(2) स्टार्च से –

ग्लूकोज के गुण :
- (I) ग्लूकोज एक एल्डोहैक्सोस है, इसे डेक्स्ट्रोस कहते है।
- (II) यह स्टार्च व सेलुलोस का एकलक है।
- (III) ग्लूकोज को HI के साथ गर्म करने पर n-Hexane देता है।
- (IV) अपचयन – ग्लूकोज सोडियम अमलगम के जलीय विलयन से अपचयित होकर सोर्विटॉल बनता है।
- (V) ग्लूकोज ब्रोमीन जल द्वारा ऑक्सीकरण से छ: कार्बन परमाणु युक्त Gluconic Acid देता है।
- (VI) ग्लूकोज, हाइड्राक्सिलऐमीन के साथ क्रिया करने पर एक ऑक्सिम देता है, तथा HCN के एक अणु के साथ सायनो हाइड्रीन देता है। ये दोनों अभिक्रिया ग्लूकोज मे कार्बोनिल समूह (>C=0) की उपस्थिति की पुष्टि में करती है।
ऑक्सीकरण:- ग्लूकोज आसानी से आक्सीकृत होता है।
(a) फेहलिग विलयन से अभिक्रिया:- फेहलिग विलयन के साथ ग्लूकोज Cu2O का लाल अवक्षेप देता है।
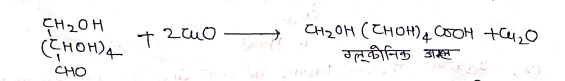
(b)टालेन अभिकर्मक के साथ:- यह रजत दर्पन देता है।

(c) निर्जलीकरण:- जब ग्लूकोज को सान्द्र सल्फ्यूरिक अम्ल के साथ गर्म करते तो कार्बन का काला अवक्षेप बनता है।

(d) सान्द्र HCl से क्रिया:- जब ग्लूकोज को सान्द्र HCl के साथ गर्म करने पर लिवलिक अम्ल बनता है

ग्लूकोज के परीक्षण
(1) ग्लूकोज को तनु NaOH के साथ गर्म करने पर पहले पीला और बाद में भूरा जाता है और अन्त मे रेजिन में बदल जाता है |
- तनु NaOH विलयन के साथ गर्म करने पर ग्लूकोज उत्क्रमनीय विन्यास द्वारा ग्लूकोज फ्रक्टोस तथा मैनोस साम्य मिश्रण बनाता है।
- यह परिवर्तन लोब्री- डी ब्राइन वान एकेन्साइटाइन पुनर्विन्यास कहलाता है।

(2) ग्लूकोज फेहलिग विलयन के साथ Cu2O का लाल अवक्षेप देता है |
(3) ग्लूकोज टॉलेन अभिकर्मक के साथ रजत दर्पण देता है।
(4) मौलिश परीक्षण:- α- नैफ्थोल का एल्कोहॉलिक विलयन को ग्लूकोज विलयन में मिलाते हैं। इसमें सान्द्र H2SO4 की कुछ मात्रा मिलाने पर लाल बैगनी रंग प्राप्त होता है
ग्लूकोज की फिशर संरचना –

ग्लूकोज की चक्रीय संरचना / फिशर प्रक्षेपण सूत्र : –

एनोमर / पाइरैनोस / हावर्थ प्रक्षेपण सूत्र :

फ्रक्टोस [C6H12O6]
- यह एक कीटो हैक्सोस होता है।
- यह ग्लूकोस के साथ मीठो फलो व शहद में पाया जाता है।
- औद्योगिक स्तर पर फ्रक्टोस को इनुलिन का तनु हाइड्रोक्लोरिक अम्ल द्वारा जल अपघटन करके बनाया जाता है।
![Class 12 Chemistry Chapter 10 Notes in Hindi जैव-अणु (PDF Download) 13 फ्रक्टोस [C6H12O6]](https://readaxis.com/wp-content/uploads/2023/03/image-557.png)
- यह सूक्रोज के जल अपघटन पर ग्लूकोज के साथ प्राप्त होता है।

भौतिक गुण:-
- (I) इसका गलनांक 1020c है।
- (II) यह जल में घुलनशील है परन्तु बेंजीन व ईथर में अघुलनशील है।
- (III) सभी शर्कराओं में फ्रक्टोज सबसे मीठा होता है।
- (IV) ग्लूकोज के समान यह भी परिवर्ती ध्रुवन घूर्णन दर्शाता है।
संरचना [C6H12O6]
- खुली श्रृंखला संरचना –
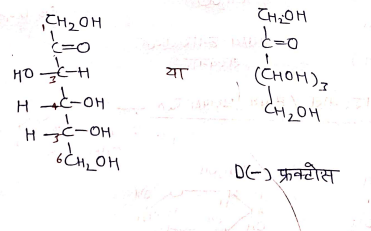
- फ्यूरिनीस संरचना –

- हावर्थ संरचना

- ओलिगोसेकराइड
सुक्रोस
- इसे cane sugar भी कहते है।
- इसका प्रमुख स्रोत गन्ने का रस शुगर वीट है।
- इसका अनुसूत्र C12H22O11 है।
- यह एक सफेद रंग का क्रिस्टलीय ठोस व H2O में विलेय है।
- यह अनअपचायक शर्करा है।
- इसका गलनांक 180oC है इसे अपने गलनांक से कुछ अधिक ताप पर गर्म करने पर यह भूरा हो जाता हैं। जिसे केरमैल कहते हैं।
- यह दक्षिण ध्रुवन घूर्णक होता है तथा परिवर्ती ध्रुवन घूर्णन प्रदर्शित नहीं करता है।
माल्टोस
इसे माल्ट शर्करा भी कहते है क्योंकि माल्ट में उपस्थिति एन्जाइम डायस्टेस द्वारा स्टार्च का जल अपघटन होकर माल्टोस बनता है।
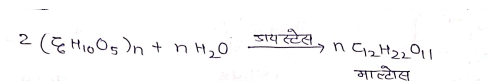
- यह एक श्वेत क्रिस्टलीय पदार्थ है।
- यह जल में विलेय परन्तु एल्कोहॉल व ईथर में अविलेय है |
- इसका गलनांक 160-165oc होता है।
- यह दक्षिण ध्रुवण घूर्णक होता है। और परिवर्ति ध्रुवण घूर्णन प्रदर्शित करता है। इसके α रूप का विशिष्ट घूर्णन +168o तथा B रूप का +112o तथा साम्प का विशिष्ट घूर्णन +136 है |
- तनु अम्ल एवं एन्जाइम माल्टेज द्वारा जल अपघटन होकर दो अणु ग्लूकोस देता है।

- यह अपचायक शर्करा है।
- माल्टोस α D ग्लूकोस क़ी दो इकाईयो से निर्मित होता है। जिसके एक इकाई का C1 व दूसरी इकाई का C4 के साथ α- ग्लाइकोसाइडिक बन्ध द्वारा जुड़ा होता है।
लैक्टोस
- लैक्टोस दुग्ध में उपस्थित होने के कारण इसे दुध शर्करा भी कहते है। इसका अणुसूत्र C12O22O11 होता है।
- यह एक श्वेत क्रिस्टलीय पदार्थ है।
- यह 203°c पर विघटन के साथ पिघलता है ।
- यह दक्षिण ध्रुवण घूर्णक है।
- लैक्टोस B-(D) गैलेक्टोस तथा B (D) ग्लूकोस से निर्मित होता है।
- यह जल में विलेय परन्तु एल्कोहॉल तथा ईथर में अविलेय है |
- गैलेक्टोस का C1 तथा ग्लूकोस का C4 के मध्य B-गलाइकोसाइड बंध बनता है । अत: यहां की ग्लूकोस C4 परमाणु एल्डिहाइड के बदलने के कारण यह भी अपचयी शर्करा है।
पाली सैकेराइड:-
(I) स्टार्च:- इसका सूत्र (C6H10O5)n होता है।
- स्टार्च पौधों में मुख्य संग्रहित पालीसैकेराइड है।
- यह α – ग्लूकोज का बहुलक है तथा दो घटको α -ऐमिलोस तथा ऐमिलोपेक्टिन से मिलकर बनता है।
- तनु अम्लो द्वारा अपघटन कराने पर यह α – ग्लूकोज देता है तथा एन्जाइम डायस्टेज द्वारा जल अपघटित होकर स्टार्च माल्टेज देता है
(II) सेलुलोस:- इसका सूत्र (C6H10O5)n है।
- यह विशिष्ट रूप से केवल पौधो में पाया जाता है
- यह वनस्पति जगत में प्रचुर मात्रा में उपलब्ध कार्बनिक पदार्थ है।
- यह पौधो की कोशिकाओ की कोशिका भित्ति का मुख्य अवयव है।
- तनु H2SO4 के साथ गर्म करने पर यह D- ग्लूकोज देता है।
- सेलुलोस B-D ग्लूकोस से बनी श्रृंखला युक्त पालीसैकेराइड है जिसमें एक ग्लूकोस इकाई के C1 तथा दूसरी ग्लूकोस के C4 के मध्य ग्लाइकोसाइडी बन्ध बनाता है।
(III) ग्लाइकोजन:- प्राणियों के शरीर में कार्बोहाइड्रेट ग्लाइकोजन के रूप में संग्रहित रहता है।
- इसकी संरचना ऐमिलोपेक्टिन के समान होती है। अत: यह भी α- D ग्लूकोज का संघनन बहुलक है।
- इसे प्राणी स्टार्च भी कहते है।
- जब शरीर को ग्लूकोस की आवश्यकता होती है तो एन्जाइम ग्लाइकोजन को ग्लूकोज में बदल देता है ।
- ग्लाइकोजन वेट पाउडर है जो जल में विलेय है तथा इसक विलयन आयोडीन से क्रिया करके बैगनी लाल रंग देता है
प्रोटीन्स(Proteins):- –
- जीव जगत में पाये जाने वाले सर्वाधिक जैव अणु प्रोटीन है। प्रोटीन के मुख्य स्रोत दूध, पनीर, दाले, मूंगफली, मछली तथा मांस आदि।
- यह शरीर के प्रत्येक भाग में उपस्थित होते है। जीवधारियो के बाल, त्वचा, नाखून, हीमोग्लोबिन, मांसपेशियां, एन्जाइम, हार्मोन आदि प्रोटीन से बने होते है।
- ये अधिकतर जलस्नेही, कोलॉइडी और उच्च अणुभार वाले जटिल जैव बहुलक होते है ।
- प्रोटीन जीवन का मूलभूत संरचनात्मक एवं क्रियात्मक आधार बनाते है।
- प्रोटीन शरीर में वृद्धि करता है एवं शारीरिक अनुरक्षण के लिए अति आवश्यक है।
- सभी प्रकार की प्रोटीन α- ऐमीनो अम्लो के बहुलक है।
प्रोटीन संघटन:- सभी प्रोटीन नाइट्रोजन युक्त जटिल कार्बनिक यौगिक है। नाइट्रोजन के अतिरिक्त C, H, S, O तत्व भी उपस्थित होते है।

प्रोटीन का वर्गीकरण:-
(1) आण्विक आधार पर प्रोटीन को दो भागो में बांटा गया है:-
(a) रेशेदार प्रोटीन:- इसमें पालीपेप्टाइड श्रृंखलाएं समान्तर होती है तथा डाइहाइड्रोजन एवं डाइ सल्फाइड आबन्धो द्वारा संयुक्त होकर रेशे जैसी संरचना बनाती है।
- ये जल में अविलेय होते हैं।
- उदा०:- किरेटिन (बाल तथा उन में), मयोसिन (मांसपेशियों में) आदि।
(b) गोलिकाकार प्रोटीन:- इसमें पालीपेप्टाइड की श्रृखलाएं कुंडली बनाकर गोलाकृति प्राप्त कर लेती है।
- ये जल में विलेय होती है |
- उदा०:- इन्सुलिन , हीमोग्लोबिन आदि ।
(2) प्रोटीन्स के जल अपघटन के आधार पर निम्न भागों में बांटा गया है –
(a) साधारण प्रोटीन:- ये प्रोटीन जल अपघटन पर केवल α- एमीनो अम्ल देती है।
उदा०→ ऐल्बुमिन, ग्लोबुलिन
(b) संयुग्मित प्रोटीन:- इनमें प्रोटीन भाग के साथ अप्रोटीन भाग भी जुड़ा रहता है, जिसे प्रोस्थेटिक समूह कहते है। संयुग्मित प्रोटीन तीन प्रकार की होती है।
- (i) न्यूक्लिओप्रोटीन:- इसमें प्रोस्थेटिक समूह न्यूक्लिक अम्ल होता है उदा०→ न्यूक्लिन
- (ii) ग्लाइकोप्रोटीन:- इसमें प्रोस्थेटिक समूह कार्बोहाइड्रेट होते है। उदा०→ माइसिन
- (iii) क्रोमोप्रोटीन :- इसमें प्रोस्थेटिक समूह कुछ वर्णक होते हैं। उदा०→ हीमोग्लोबिन, क्लोरोफिल
एमीनो अम्ल (Amino Acid)
ऐमीनो अम्लो में ऐमीनों (-NH2) तथा कार्बोक्सिलिक (- COOH) समूह उपस्थित होता है।

- प्रोटीन के जल अपघटन से केवल α- एमीनो अम्ल ही प्राप्त होते है।
- ऐमीनो अम्लो में अन्य समूह भी उपस्थित हो सकते है।
- ग्लाइसीन (Glycine) को उसका नाम मीठे स्वाद के कारण दिया जाता है।
- कुल ऐमीनो अम्लो की संख्या 20 है।
ऐमीनो अम्लो का वर्गीकरण:-

(1) कार्य के आधार पर:-
(a) आवश्यक ऐमीनो अम्ल:- इस वर्ग में उन ऐमीनो अम्लो को रखा गया है, जिनकी जीवधारियो को सख्त आवश्यकता होती है। इनकी शरीर मे कमी से शारीरिक वृद्धि रुक जाती है और मृत्यु तक हो जाती है।
- इनकी संख्या 10 है तथा ये थ्रिओन्नीन, वैलीन, ल्युसीन, आइसोल्युसीन, लाइसीन, मेथिइओनिन, फेनिल- एलेनिन, ट्रिप्टोफेन आर्जिनिन और हिस्टिडीन है।
- इसे संक्षिप्त में TVMILL PATH से प्रदर्शित करते है।
(b) अनावश्यक ऐमीनो अम्ल:- इस वर्ग में उन ऐमीनो अम्लो को रखा गया है जिनके अभाव से कोई भी विपरीत प्रभाव नहीं पड़ता है। 10 आवश्यक ऐमीनों के अलावा शेष इस वर्ग में आते है।
(2) प्रकृति के आधार पर –
(a) अम्लीय ऐमीनो अम्ल:- इसमें एक एमीन समूह और दो कार्बोक्सिलिक समूह पाये जाता है। इसीलिए इनकी प्रकृति अम्लीय होती है।
उदा०→ एस्पार्टिक अम्ल, ग्लूटैमिक अम्ल आदि।
(b) क्षारीय ऐमीनो अम्ल:- इसमें दो एमीन समूह व एक कार्बोक्सिलिक समूह पाये जाता है।इसीलिए इनकी प्रकृति क्षारीय होती है।
उदा० → लाइसीन, आर्जिनिन, हिस्टिडीन, ट्रिप्टोफेन आदि।
(c) उदासीन ऐमीनो अम्ल:- इसमें दो एमीन समूह और एक कार्बोक्सिलिक समूह पाया जाता है। इसीलिए इनकी प्रकृति उदासीन होती है।
उदा० → ग्लाइसीन, वैलीन, ऐलेनीन आदि।
(3) ऐमीनो समूह की स्थिति के आधार पर:-
(a) α- एमीनो अम्ल:- इनमें ऐमीनो समूह कार्बोक्सिलिक समूह से α स्थिति पर होता है अर्थात दोनो समूह एक ही कार्बन से जुड़े रहते हैं।
उदा०

(b) β- एमीनो अम्ल:- इसमें स्थिति समूह कार्बोक्सिलिक समूह से β स्थिति पर होता है।

(c) Y – एमीनो अम्ल:- इसमें ऐमीनो समूह कार्बोक्सिलिक समूह से Y स्थिति पर होता है।
उदा०

एमीनो अम्लो के गुणधर्म –
(1) गलनांक: इनमें अम्लीय व क्षारीय दोनों समूह होने के कारण इनमें अन्तराअणुक बल प्रबल होते है। इसीलिए इनके गलनांक उच्च होते है।
(2) ज्विटर आयन:– अम्लीय कार्बोक्सिलिक अम्ल व क्षारीय ऐमीनो दोनो प्रकार के समूहो की उपास्थिति के करण ,एमीनो अम्लो में द्विध्रुवीय संरचना पाई जाती है जिसे ज्विटर आयन कहते हैं।
(3) विलेयता:- ये रंगहीन व क्रिस्टलीय ठोस है। ये जल, अम्ल और क्षारो में विलेय होते है। परन्तु कार्बनिक विलायको अल्प विलेय होते हैं |
(4) असममित C परमाणु :- ग्लाइसिन के अलावा अन्य सभी एमीनो अम्लो में एक असममित C परमाणु पाया जाता है। इसीलिए ये प्रकाशिक समावयवता प्रदर्शित करते हैं।
(5) समविभव बिन्दु:- वह PH जिस पर एमीनो अम्ल विद्युत क्षेत्र से अप्रभावित रहता है तथा इसकी रासायनिक क्रियाशीलता स्थिर हो जाती है, समविभव बिन्दु कहलाती है। प्रत्येक एमीनो अम्ल में इसका मान निश्चित होता है। जिस PH पर समविभव बिन्दु प्राप्त होता है।
एमीनो अम्लो का महत्व:-
- (1) ये शरीर की वृद्धि के लिए अत्यंत जरूरी है।
- (2) इनसे पेप्टाइड व प्रोटीन का निर्माण होता है।
- (3) ये शरीर से विषैले पदार्थो को निष्कासित करने में सहायता करते है।
- (4) इनमें हार्मोन का निर्माण होता है।
पेप्टाइड बन्ध – एक एमीनो अम्ल के – NH2 समूह और दूसरे एमीनो अम्ल के कार्बोक्सिलिक समूह के मध्य संघनन सें H2O अणु बाहर निकलता है तथा इनके मध्य जो बन्ध बनता है उसे पेप्टाइड बन्ध कहते है। इस बन्ध को -Co-NH- द्वारा प्रदर्शित करते हैं।
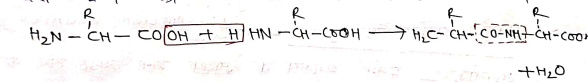
एमीनो अम्लो की संख्या के आधार पर पेप्टाइडो को चार भागों में बांटा गया है:-
- (I) डाईपेप्टाइड → दो एमीनो अम्ल परस्पर जुड़े होते हैं।
- (II) ट्राईपेप्टाइड → तीन एमीनो अम्ल परस्पर जुड़े होते है।
- (III) टेट्रापेप्टाइड → चार एमीनो अम्ल परस्पर जुड़े होते हैं।
- (IV) पालीपेप्टाइड → इनमें अनेक एमीनो अम्ल परस्पर जुड़े रहते हैं।
प्रोटीन
- प्रोटीन वास्तव में पालीपेप्टाइड होते हैं। इनका निर्माण अनेको ऐमीनो अम्लो के मध्य संघनन से होता है। प्रोटीन जल अपघटित होकर एमीनो अम्ल देती है।
(1) प्रोटीन की संरचना
प्राथमिक संरचना:-
- विभिन्न एमीनो अम्लो के परस्पर रेखीय क्रम में पेप्टाइड बंघ द्वारा जुड़ने से प्रोटीन की प्राथमिक संरचना का निर्माण होता है।
- प्राथमिक संरचना द्वारा एमीनो अम्ल की प्रकृति संख्या और इनकी व्यवस्था की जानकारी प्राप्त होती है।
- प्रोटीन की प्राथमिक संरचना में पेप्टाइड बन्ध, हाइड्रोजन बन्ध और डाई सल्फाइड बन्ध पाये जाते है।
- प्रोटीन की प्राथमिक संरचना निम्न प्रकार से दर्शाते है –

- Z1 व Z2 α- एमीनो अम्ल में उपस्थित विभिन्न समूह है।
(2) द्वितीयक संरचना:-
- प्रोटीन के द्वितीयक संरचना की जानकारी पॉलिंग और कोरे नामक वैज्ञानिक ने दी थी।
- द्वितीयक संरचना प्रोटीन में पालीपेप्टाइड श्रृंखलाओ की व्यवस्था के प्रति जानकारी प्राप्त होती है।
→ α- हेलिक्स संरचना:- प्रोटीन की इस संरचना में पालीपेप्टाइड श्रृंखलाएं मुड़े हुए रिबन की भांति सर्पिलाकार होकर हेलिक्स संरचना बनाती है। फलस्वरूप प्रत्येक ऐमीनो अम्ल अवशिष्ट का – NH समूह कुण्डली के अगले मोड़ पर स्थित >C-O समूह के साथ हाइड्रोजन आबन्ध बनता है |
ये प्रोटीन लचीले होते है तथा खीचे जा सकते है। छोड़ने पर अपने पूर्व स्थित में चले जाते हैं |
→ यदि पॉलीपेप्टाइड श्रृंखलाएं परत के समान व्यवस्थित होकर ये परते एक के ऊपर एक व्यवस्थित हो तो उसे बीटा (β) प्लेट संरचना कहते हैं। इस प्रकार की संरचना पाली प्रोटीन मुलायम होती है। जैसे- रेशम ।
→ द्वितीयक संरचना में विभिन्न पालीपेप्टाइड श्रृंखलाओ के मध्य हाइड्रोजन बन्ध, ऐमाइड बन्ध, डाईसल्फाइड बन्ध आदि स्थापित हो जाते है।
प्रोटीन के अणु की द्वितीयक संरचना –

(3) तृतीयक संरचना :-
प्रोटीन की तृतीयक संरचना त्रिविमीय होती है|

- विभिन्न द्वितीयक पालीपेप्टाइड श्रृंखलाओ के विशिष्ट स्थान पर मुड़कर व लुप बनाकर, परस्पर अन्तराबन्ध बना लेती है। अत: पालीपेप्टाइड श्रृंखलाये गुच्छित होकर एक निश्चित संघनन आकृति में व्यवस्थित हो जाती है, जिसे प्रोटीन की तृतीयक संरचना कहते है ।
- तृतीयक संरचना प्रोटीन अणु का सम्पूर्ण आकार निर्धारित किया जाता है।
- गोलाकार प्रोटीन जैसे – हीमोग्लोबिन (या मामोग्लोबिन) की संरचना कुण्डली के आकार की होती है|
(4) प्रोटीन का चतुष्क संरचना:-
दो या दो से अधिक पालीपेप्टाइड श्रृंखलाएं मिलकर प्रोटीन की चतुष्क संरचना का निर्माण करती है।
- ये श्रृंखलाएं हाइड्रोजन बन्ध, वैधुत संयोजी आकर्षण तथा वाण्डर वाल आकर्षण बल द्वारा संयोजित रहती है।
- उदा०:- आइसोजाइम, हीमोग्लोबिन [2α, 2B]
प्रोटीन का विकृतिकरण :- प्रोटीन को गरम करने पर या इनमें अम्ल या क्षार अथवा भारी धातु लवण मिलाने पर ये नष्ट या विकृत हो जाती है। इसे विकृतिकरण कहते है।
विकृतीकरण की प्रक्रिया में प्रोटीन की द्वितीयक व तृतीयक संरचनाये नष्ट हो जाती है परन्तु प्राथमिक संरचना में कोई परिवर्तन नहीं होता है ।
विकृतिकरण दो प्रकार का होता है –
- (I) उत्क्रमणीय विकृतिकरण
- (II) अनुत्क्रमणीय विकृतिकरण
प्रोटीन का परीक्षण
- (1) बाड्यूरेट परीक्षण:- प्रोटीन को 10% NaOH विलयन के साथ गर्म करके, इसमें थोड़ा सा CuSO4 विलयन मिलाने पर भूरे बैगनी रंग का विलयन प्राप्त होता है।
- (2) जैन्थोप्रोटिक परीक्षण:- प्रोटीन, सान्द्र HNO3 के साथ गर्म करने पर पीला रंग देती है। NH4OH मिलाने पर यह नारंगी हो जाता है।
प्रोटीन का उपयोग :-
- (1) एन्जाइन तथा हार्मोन संश्लेषण
- (2) पेशियो का निर्माण
- (3) शरीर की वृद्धि तथा क्षतिग्रस्त कोशिकाओ तथा ऊतको में सुधार करना।
- (4) एण्टीबाडी के रूप में शरीर की सुरक्षा प्रदान करना
- (5) आनुवंशिक लक्षणों के विकास आदि ।
एन्जाइम (Enzyme):-
एन्जाइम को सर्वप्रथम खमीर कोशिकाओ से प्राप्त किया गया था अत: इन्हें एन्जाइम कहते हैं।

मुख्यतः ये जैव रासायनिक अभिक्रियाओ मे भाग लेते है। अत: ये जैव रासायनिक उत्प्रेरक भी कहते है।
एन्जाइमो के नामकरण:-
एन्जाइंम जिस पदार्थो पर क्रिया करते है उन्हें क्रियाधार कहते है एवं एन्जाइमो का नामकरण उनके क्रियाधार के नाम के अन्त में ‘एज’ लगाकर करते है।
जैसे -> यूरिएज => यूरिया पर क्रिया करता है।
एन्जाइमों का वर्गीकरण :
(1) ऑक्सिडोरिडक्टेस:- मनुष्य के जीवित ऊतको की उत्पादक अभिक्रियाओ में भाग लेने वाले एन्जाइम आक्सिडोरिडक्टेस कहलाते है | ये एन्जाइम स्थानान्तरण इलेक्ट्रॉन तथा H+ आयनो के स्थानान्तरण पर कार्य करते हैं।
उदा०→

(2) ट्रांसफिरेस:- परमाणुओ के समूहो का एक अणु से दूसरे अणु पर स्थानान्तरण की क्रियाविधि पर आधारित एन्जाइम ट्रांसफिरेस कहलाते है |
(3) हाइड्रोलेस:- ये एन्जाइम बड़े तथा जटिल अणुओ को विघटित करके उनमे जल का संयोजन कर देते है। उदा०→

(4) लाइऐज:- ये दो प्रकार से कार्य करते हैं –
- (I)परमाणुओ के समूह से क्रियाधार के द्विक बन्धो को हटाना।
- (II) परमाणुओ के समूहो का क्रियाधार के द्विक बन्धो पर योग ।
(5) आइसोमरेज:- क्रियाधार मे परमाणुओ को अत्त: अणुक विन्यास प्रदान करने वाली अभिक्रियाओ को उत्प्रेरित करने वाला एन्जाइम आइसोमरेज कहलाता है।
(6) लाइगेस:- ये एन्जाइम उन अभिक्रियाओ को उत्प्रेरित करते हैं, जिनमें ATP के पायरोफॉस्फेट बंध का विखण्डन होता है तथा दो अणुओ के मध्य बन्ध बनता है।
एन्जाइम की क्रियाविधि
- एन्जाइम जैव रासायनिक अभिक्रियाओ की गति में वृद्धि करते हैं किन्तु अन्त में स्वयं अपरिवर्तित रहते हैं।
- एन्जाइम सक्रियण ऊर्जा (Activation Energy) को कम कर देते है जिसके फलस्वरूप निम्न तापक्रम पर भी अभिक्रियाओं गति बढ़ जाती हैं।
एन्जाइम की क्रियाविधि निम्न पदो में होती है –
पद-1: एन्जाइम तथा क्रियाधार (Substance) की क्रिया से संबुल निर्माण:-

पद-2: उपरोक्त संकुल का एन्जाइम मध्यवर्ती संकुल में परिवर्तन –

पद-3:- EI का उत्पाद संकुल (EP) में परिवर्तन –
EI -> EP
पद -4: एन्जाइम संकुल उत्पाद (EP), का एन्जाइम तथा उत्पाद में विघटन:-

एन्जाइम के गुणधर्म-
- (1) अधिकांश एन्जाइम रंगहीन तथा जल एवं लवणो के तनु विलयनो में विलेय होते है।
- (2) रासायनिक दृष्टि से एन्जाइम प्रोटीन के बने होते है। (RNA के अलावा)
- (3) एन्जाइम अभिक्रिया में कभी समाप्त नहीं होते हैं।
- (4) किसी भी अभिक्रिया के लिए एन्जाइम की बहुत थोड़ी मात्रा पर्याप्त होती है क्योंकि ये पुनः प्रयुक्त हो सकते है।
- (5) एन्जाइम किसी भी अभिक्रिया की सक्रियण ऊर्जा को कम करके अभिक्रिया की गति बढ़ाते है तथा इनकी उपस्थिति से अभिक्रिया की दर 1020 गुणा तक बढ़ जाती है।
- (6) एन्जाइम अभिक्रिया की दिशा अथवा साम्यावस्था पर इसका कोई प्रभाव नहीं पड़ता।
- (7) एन्जाइम शरीर तापमान (310K) तथा सामान्य PH (6-Q) पर अधिक सक्रिय होते है।
- (8) एन्जाइम अतिविशिष्ट होते है।
- (9) उच्च ताप, पराबैगनी प्रकाश, उच्च लवण सान्द्रता व क्षारीय अभिकर्मक एन्जाइम की प्रकृति, स्थिति तथा संरचना को विकृत कर देते है इसे विकृतिकरण कहते हैं। इससे एन्जाइम की सक्रियता समाप्त हो जाती है
- (10) कुछ कृत्रिम अणु भी एन्जाइम जैसी उत्प्रेरक क्रियाएं दिखाते है उन्हें कृत्रिम एन्जाइम कहते है।
- एन्ज़ाइम की उपयोगिता –
- (1) पाचन प्रक्रिया के उत्प्रेरण में।
- (2) उद्योगो के कई पदार्थो जैसे-मदिरा, चमड़े के परिरक्षण में।
- (3) रोगो के उपचार में ।
- (4) स्ट्रेप्टोकाइनेज एन्जाइम रक्त का थक्का बनने से रोकने में ।
- (5) दूध के स्कन्दन से पनीर निर्माण में आदि ।
हार्मोन (Hormones):-
कोशिकाओ के मध्य संदेशवाहक का कार्य करने वाले वे रासायनिक पदार्थ जो अत:स्रावी ग्रंथियों से स्त्रावित होते है। हार्मोन कहलाते हैं।
ये जैव रासायनिक अभिक्रियाओ को प्रभावित एवं नियंत्रित करते है।
हार्मोन के प्रकार:- ये मुख्यतः तीन प्रकार के होते है –
(1) पेप्टाइड हार्मोन – उदा० -> इन्सुलिन, ग्लूकैमान, ऑक्सीटोसिन, वैसोप्रेसिन ।

(2) स्टेरॉयड हार्मोन – उदा० -> टेस्टोस्ट्रीएन, एस्ट्रोजन, प्रोजेस्टीयन कीर्टीसोन |
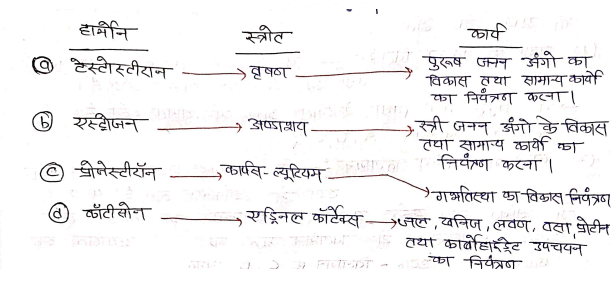
(3) ऐमीन हार्मोन – उदा० -> थायरॉक्सिन, एड्रिनेलीन |

विटामिन
- विटामिन की खोज फंक ने 1920 में की थी।
- प्रोटीन, कार्बोहाइड्रेट तथा वसा के अतिरिक्त वे कार्बनिक यौगिक जो सामान्य स्वास्थ्य, शरीरिक वृद्धि एवं पोषण व पाचन क्षमता को बनाये रखने के लिए आवश्यक होते है, विटामिन कहलाते है।
- विटामिन मानव शरीर में निर्मित नहीं होते है अत: ये अतिरिक्त आहार कारक भी कहलाते हैं ।
Vitamin → vital + amine
विटामिन का वर्गीकरण
विलेयता के आधार पर विटामिन दो प्रकार के होते है –
(1) वसा में विलेय विटामिन:- ये विटामिन जल मे अविलेव परन्तु वसा एवं तेल में विलेय होते हैं।
- ये यकृत तथा (वसा) ऐडियोस ऊतक में संचित रहते हैं।
- उदा०:- विटामिन A, D, E, K
(2) जल में विलेय विटामिन:- ये विटामिन जल में विलेय तथा वसा में अविलेय होते हैं। ये शरीर में संचित नहीं रहते अत: इन विटामिनो को लगातार लेते रहना चाहिए। ये विटामिन मूत्र के साथ उत्सर्जित हो जाते है। उदा० – विटामिन B, C, D आदि।
Note:- जल में विलेय विटामिन B12 शरीर में सचित रहता है।

न्यूक्लिक अम्ल (Nuclic Acid):-
न्यूक्लिक अम्ल (Nuclic Acid):- जीव कोशिका के नाशिक में उपस्थित वह कण जो आनुवांशिकता के लिए उत्तरदायी होते है, क्रोमोसोम कहलाते हैं जो कि प्रोटीन तथा अन्य जैव अणुओं से मिलकर बने होते हैं, न्यूक्लिक अम्ल कहलाते है।
- न्यूक्लिक अग्ल C, H, O, N व P के जटिल कार्बनिक यौगिक होते है। ये मुख्यतः केन्द्रक में पाये जाते है|
- ये न्यूक्लियोटाइडो की लम्बी श्रृंखला वाले बहुलक होते है अत: इन्हें पॉलिन्यूक्लियोटाइड भी कहते है।
ये दो प्रकार के होते है-
- (1) डी आक्सी राइबोन्यूक्लिक अम्ल (DNA)
- (2) राइबोन्यूक्लिक अम्ल (RNA)
न्यूक्लिक अम्ल की संरचना:-
न्यूक्लिक अम्ल रंगहीन ठोस है। जो छोटे जैव अणुओ से मिलकर बनते हैं। वे पूर्ण जल अपघटन पर फॉस्फोरिक अम्ल, शर्करा व क्षार देते है।
अत: न्यूक्लिकं अम्ल के तीन घटक होते है –
- (I) फॉस्फोरिक अम्ल
- (II) शर्करा
- (III) नाइट्रोजनी कार्बनिक क्षार
(I) फास्फोरिक अम्ल या फास्फेट समूह –

(II) शर्करा:- न्यूक्लिक अम्ल के जल अपघटन पर दो शर्कराए D (-) राइबोस तथा 2- डीऑॉक्सी (D-) राइबोस प्राप्त होती है।
राइबोस शर्करा RNA में व डी-ऑक्सी राइबोस शर्करा DNA में पायी जाती है।

(III) नाइट्रोजन युक्तक्षार:- ये दो प्रकार के होते हैं।
- (a) प्यूरीन
- (b) पिरीमिडीन
(I) प्यूरीन :- ये दो प्रकार के होते हैं
- (a) एडिनीन (A)
- (b) गुआनिन (G)

(II) पिरीमिडीन – ये तीन प्रकार के होते है:-
- (a) यूरेसिल (U)
- (b) थायमीन (+)
- (c) साइटोसीन (C)
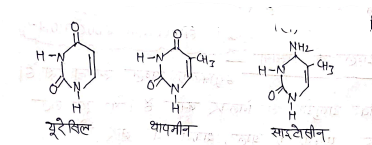
Note-> थायमिन केवल DNA में व यूरेसिल केवल RNA में पाया जाता है। बाकी तीनों क्षार दोनों में पाये जाते है।
न्यूक्लिओसाइड व न्यूक्लिओटाइड :-
- एक क्षार व शर्करा के परस्पर बन्धित होकर बनने वाला अणु न्यूक्लिओसाइड कहलाता है।
- न्यूक्लिओसाइड तथा फॉस्फेट समूह से बनी इन्काई न्यूक्लिओटाइड कहलाती है |
- न्यूक्लिओसाइड:- कार्बनिक क्षार + शर्करा
उदा० ->

एडीनोसीन
न्यूक्लिओटाइड (फास्फेट समूह + न्यूक्लिओसाइड)
अनेक न्यूक्लिओटाइड की इकाईया आपस में मिलकर एक श्रृंखला बनाती है जिसे न्यूक्लिक अम्ल कहते हैं।

एडीनाइलिक एसिड

न्यूक्लिक अम्ल की प्राथमिक संरचना:-
न्यूक्लिक अम्ल की वह संरचना जो उसमें शर्करा, फास्फेट तथा नाइट्रोजन क्षार के परस्थर जुड़ने के विशिष्ट अनुक्रम को दर्शाती है, प्राथमिक संरचना कहलाती है।

DNA की द्वितीयक संरचना:- जेम्स वाटसन तथा फैन्सिल क्रिक ने DNA की द्वितीयक संरचना के बारे में बताया ।
इनके अनुसार DNA में न्यूक्लिक अम्ल की दो पालीपेप्पटाइड श्रृंखला विपरीत रूप से समान्तर व्यवस्थित होकर कुण्डलीत रहती है तथा इनके क्षार युग्मो में H – बन्ध पाया जाता है।
एक कुण्डली की गुआनिन दूसरी कुण्डली के साइटोसीन से 3 H- बन्ध द्वारा जुड़ी रहती है। इसी प्रकार एक कुण्डली की एडीनीन दूसरी कुण्डली के थायमीन से 2H- बन्ध द्वारा जुड़ी होती है। इस कारण यह सबसे स्थायी संरचना है।
इसे DNA का द्विकुण्डलीय त्रिविगीय संरचना या वाटसन क्रिक संरचना कहते है|
कुण्डली के प्रत्येक चक्र में 34oA की दूरी तथा एक चक्कर में 10 न्यूक्लिओटाइड युग्म होते हैं।
DNA का व्यास 20oA में होता है।
क्षार युग्मो के बीच की दूरी 3.4oA होती है।
शर्करा के अणुओं के बीच की दूरी 11oA होती है।

कार्यात्मक विशिष्टा के आधार पर RNA के प्रकार
- (1) संदेश वाहक RNA (m-RNA):- प्रोटीन संश्लेषन में टेम्प्लेट की भाँति कार्य करता है।
- (2) अंतरण RNA (t – RNA) – ये अवयवी अम्लो को m-RNA टक लाने का कार्य करते हैं।
- (3) राइबोसोमल RNA (r– RNA) – एमीनो अम्लो को पेप्टाइड बन्ध द्वारा जोड़ने में सहायक है ।
| DNA | RNA |
|---|---|
| (1) यह केन्द्र में पाये जाने वाले गुणसूत्र में पाया जाता है। | (1) यह मुख्यतः कोशिका द्रव्य में पाया जाता है। |
| (2) इसमें डी-ऑक्सीराइबोस शर्करा होती हैं। | (2) इसमें राइबोस शर्करा पायी जाती है। |
| (3) DNA में क्षार ऐडीनीन, ग्वानीन, थायमीन तथा साइटोसीन पाये जाते है। | (3) RNA में और ऐडीनीन ग्वानीन, यूरेसील तथा साइटोसीन पाये है। |
| (4) यह आनुवांशिक गुणो के स्थानान्तरण में महत्वपूर्ण भूमिका अदा करता है। | (4) यह प्रोटीन संश्लेषण में मदद करता है। |
न्यूक्लिक अम्लो के जैविक कार्य –
जैव शरीर में DNA दो प्रमुख कार्य करता है-
(1) प्रतिकृति (Replication):- DNA के विशेष गुण के कारण इसका एक अणु विभाजित होकर दो समान प्रतिलिपियां बनाता है यह प्रक्रिया प्रतिकृति कहलाती है।
- इस प्रक्रिया में DNA की द्विकुण्डलीय संरचना खुलकर नई श्रृंखलाओ के दो पैटर्न बनाती है, जिसे संतति DNA कहते है। फिर प्रत्येक स्टैण्ड पर उचित न्यूक्लिपोटाइड जुड़ते है और समरूप संतति द्विकुण्डलिनी बन जाती है।
- इसी प्रकार प्रत्येक संतति द्विकुण्डलीय के एक कुण्डली जनक DNA से आती है तथा दूसरी कुण्डली नई बनी होती है। जिन्हें क्रमश: जनक स्ट्रैण्ड तथा संतति स्टैण्ड कहते है।
(2) प्रोटीन संश्लेषण नियंत्रण:- कोशिका में प्रोटीन संश्लेषण विभिन्न RNA अणुओं द्वारा होता है परन्तु किसी विशेष प्रोटीन के संश्लेषण का संदेश DNA के पास होता है अत: प्रोटीन संश्लेषण पर DNA का नियंत्रण होता है।
DNA Finger printing:-
- प्रत्येक व्यक्ति का एक निश्चित DNA पैटर्न होता है जो किसी भी अन्य व्यक्ति से अलग होता है जो DNA अणुओं में क्षार के विशिष्ट अनुक्रम के कारण होता है।
- व्यक्ति की पहचान के लिए DNA फिंगरप्रिन्ट का प्रयोग करते हैं।
- किसी व्यक्ति के DNA पैटर्न से सम्बन्धित सूचना DNA Fingerprint कहलाता है तथा यह तकनीक DNA Fingerprinting कहलाती है।
DNA का महत्व
- (I) DNA आनुवांशिक वाहक की तरह कार्य करता है।
- (II) यह जीवो की पीढ़ी दर-पीढी नियंत्रण करता है।
- (III) यह आनुवांशिकता की इकाई होती है।
Chapter 8 – ऐल्डिहाइड, किटोन एवं कार्बोक्सिलिक अम्ल नोट्स
Chapter 9 – एमीन
Tagged with: Bio Molecules notes in hindi | Chemistry chapter 10 class 12 notes in hindi | Chemistry class 12 chapter 10 in hindi notes | Chemistry class 12 chapter 10 notes in hindi | class 12 Chemistry chapter 10 ncert notes in hindi | Class 12 Chemistry Chapter 10 Notes in Hindi

ऐमआइलओ पेक्टिन की हावर्ड संरचना
Chemistry
surface chemistry wala handwriting mast hai