यहाँ हमने Class 12 Chemistry Chapter 7 Notes in Hindi दिये है। Class 12 Chemistry Chapter 7 Notes in Hindi आपको अध्याय को बेहतर ढंग से समझने में मदद करेंगे और आपकी परीक्षा की तैयारी में सहायक होंगे।
Class 12 Chemistry Chapter 7 Notes in Hindi
एल्कोहॉल (Alcohol):- ऐल्केनो के हाइड्राक्सी व्युत्पनो को एल्कोहॉल कहते है .
किसी एल्केन अणु से एक या एक से अधिक हाइड्रोजन परमाणुओ को हाइड्रॉक्सी समूहो (OH–) द्वारा प्रतिस्थापित करने पर एल्कोहॉल प्राप्त होता है।

एल्कोहॉल का वर्गीकरण :
(a) OH समूहो की संख्या के आधार पर –
(i) मोनोहाइड्रिक एल्कोहॉल:- इसमें केवल एक OH समूह उपस्थित होता है।
- उदा० (i) CH3OH (मेथिल एल्कोहॉल)
- (ii) CH3 – CH2OH (एथिल एल्कोहॉल)
(ii) डाइहाइड्रिक एल्कोहॉल:- इसमें दो OH समूह अलग-अलग C पर उपस्थित होते है।

(iii) ट्राईहाइड्रिक एल्कोहॉल:- इसमें तीन OH समूह अलग-अलग C पर उपस्थित होते है। उदा०

(iv) पॉलीहाइड्रीक ऐल्कोहॉल:- इसमें तीन से अधिक OH समूह उपस्थित होते है।
उदा०-

(b) कार्बन परमाणु की प्रकृति के आधार पर:-
(i) प्राथमिक एल्कोहॉल:- OH– समूह 10C परमाणु पर उपस्थित होता है।

(ii) द्वितीयक एल्कोहॉल:- OH समूह 20C परमाणु से जुड़ा होता है।

(iii) तृतीयक एल्कोहॉल:- OH समूह 3°C परमाणु से जुड़ा होता है।

एल्कोहॉलो का नामकरण
एल्कोहॉलो के नामकरण तीन प्रकार के होते है:-
- (a) साधारण नाम
- (b) व्युत्पन्न नाम
- (c) IUPAC नाम
(a) साधारण नाम:- एल्कोहॉल का रूढ़ नाम या साधारण नाम ऐल्किल एल्कोहॉल होता है जिसे प्राप्त करने के लिए उसके संरचनात्मक सूत्र में विद्यमान ऐल्किल मूलक के नाम के अन्त में एल्कोहॉल लिख देते है। उदा०

(b) व्युत्पन्न नाम:- एल्कोहॉलो के व्युत्पन्न नाम प्राप्त करने के अपनायी गयी पद्धति को कार्बोनाल पद्धति (carbinol system) कहते हैं। इसके अनुसार – CH2-OH को केवल कार्बिनाल (carbinol) कहा जाता है। उदा०

(c) IUPAC नाम:- ऐल्कोहॉलो के IUPAC नामकरण के लिए OH समूह के लिए अनुलग्न ऑल (ol) का प्रयोग किया जाता है। OH समूह युक्त मूल श्रृंखला के जनक ऐल्केन नाम की सन्धि ऑल के पहले कर दी जाती है।
- आवश्यक होने पर मूल श्रृंखला का क्रमांकन इस प्रकार किया जाता है कि OH समूह को न्यूनतम स्थिति क्रमीक मिले।
- पार्श्व श्रृंखलाएं होने पर उनके नाम पूर्वलग्नो के रूप में अंग्रेजी वर्णक्रमानुसार लिखे जाते है। उदा०-
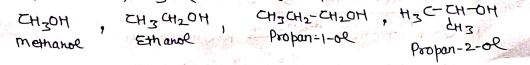
- कुछ एल्कोहॉलो के व्यापारिक नाम –

एल्कोहॉल (R-OH) बनाने की विधियाँ :-
- हैलोऐल्केन के जल अपघटन द्वारा
- ग्रिगनाई अभिकर्मक से:
- ईथर के जल अपघटन द्वारा
- एस्टर के जल अपघटन द्वारा –
- अपचयन द्वारा एल्कोहॉल का निर्माण
- जल गैस से
एल्कोहॉलो के भौतिक गुण:-
- एल्कोहॉल परिवार के प्रथम तीन सदस्य (CH3OH, C2H5OH, C3H7OH) मीठी गंध वाले रंगहीन द्रव है।
- C4H9OH से C11H23OH तक के सदस्य तेल के समान गाढे द्रव है।
- एल्कोहॉल अणुओ के मध्य प्रबल हाइड्रोजन आबन्ध उपस्थित होने के कारण एल्कोहॉल का क्व्थनांक समान अणुभार वाले ऐल्केनो तथा ईथर की अपेक्षा अधिक होता है।
- अणुभार मे वृद्धि के साथ पृष्ठ क्षेत्रफल मे वृद्धि होने के कारण वाण्डर वाल्स बल मे भी वृद्धि हो जाती है। जिस कारण क्वथनांक बंढ जाता है।
- एथिल एल्कोहॉल निर्जल CaCl2 के साथ अभिक्रिया करके क्रिस्टलीय ठोस CaCl2 .4C2H5OH बनाता है। इसी कारण एथिल एल्कोहॉल को शुष्क करने के लिए निर्जल CaCl2 का प्रयोग नही किया जा सकता।
रासायनिक गुण-
(1) ग्रिगनाई अभिकर्मक से क्रिया – [R-Mg X]

(2) एल्कोहॉल का अम्लीय व्यवहार
- अम्ल + सक्रिय धातु → लवण + हाइड्रोजन
- अम्ल + क्षार → लवण + जल
(3) फिशर एस्टरीकरण

(4) एल्कोहॉल का हैलोजन अम्ल से अभिक्रिया

(5) ऐल्कोहॉल की PCl3/pCl5 से अभिक्रिया –

(6)ऐल्कोहॉल का निर्जलन

(7) एल्कोहॉल की थायोनिल क्लोराइड से अभिक्रिया –

(8) एल्कोहॉल का ऑक्सीकरण:- O जुड़ना या H निकलना
- दुर्बल या मृदु आवसीकारक → PCC= C5H5NHClCrO3 PDC = (C5H5NH)2Cr2O7
- प्रबल ऑक्सीकारक → KMnO4/H+, KMnO4/OH–, KMnO4/उदासीन , K2Cr2O7/H+

Note=>3oC एल्डिहाइड का ऑक्सीकरण नहीं होता है।
(9) HNO3 से क्रिया:- CH3OH + HNO2 → CH3ONO2 + H2O
(10) HNO2 से क्रिया:- CH3OH + HNO2 → CH3ONO + H2O
(11) बेंजायलीकरण / शॉटन बाउमन अभिक्रिया:-

प्राथमिक द्वितीयक तथा तृतीयक एल्कोहॉल में विभेद :-
इसकी निम्न विधियां है:-
(1) ऑक्सीकरण विधि:- इस विधि मे दिये गये एल्कोहॉल का ऑक्सीकरण किया जाता है तथा ऑक्सीकरण से प्राप्त उत्पाद की पहचान की जाती है।
(2) विक्टर मेयर विधि:- इस विधि में दिये गए एल्कोहॉल को क्रम से फास्फोरस तथा आयोडीन, सिल्टर नाइट्राइट, नाइट्स अम्ल तथा NaOH से अभिकृत कराते हैं।
- यदि एल्कोहॉल प्राथमिक होता है तो रक्त जैसा लाल रंग प्राप्त होता है।
- यदि एल्कोहॉल द्वितीयक है तो नीला रंग प्राप्त होता है।
- यदि एल्कोहॉल तृतीयक है तो रंग में कोई परिवर्तन नहीं होगा।
(3) ल्यूकॉस परीक्षण:-
- सान्द्र HCl तथा निर्जल ZnCl2 के मिश्रण को ल्यूकॉस अभिकर्मक कहते है।
- ऐल्कोहॉल ल्यूकॉस अभिकर्मक से इस प्रकार अभिक्रिया करते है कि उनमे उपस्थित OH समूह – Cl द्वारा विस्थापित जाते है
- यह अभिक्रिया तृतीयक एल्कोहॉलो के साथ कमरे के ताप पर ही तेज गति से होती है, द्वितीयक एल्कोहॉल के साथ कमरे के ताप पर मंद गति से होती हैं तथा प्राथमिक एल्कोहॉल के साथ कमरे के ताप पर होती ही नहीं है।
- अभिक्रिया के फलस्वरूप क्लोरो यौगिक बनने के कारण तैलीय द्रव या सफेद अविलेयता प्राप्त होती है।
- अत: किसी अज्ञात एकोहॉल में ल्यूकास अभिकर्मक मिलाने पर तुरन्त ही तैलीय द्रव या सफेद अविलेयता प्राप्त होती है तो यह एक तृतीयक एल्कोहॉल है
- यदि कुछ समय बाद प्राप्त हो तो उसे द्वितीयक एल्कोहॉल कहते हैं।
- यदि कमरे के ताप पर तैलीय द्रव या सफेद अविलेषता प्राप्त नहीं होती है तो यह एक प्राथमिक एल्कोहॉल है।
(1) मेथेनाल
रासायनिक सूत्र – CH3OH
इसे लकड़ी के भंजक आसवन द्वारा प्राप्त किया जाता है । इसीलिए इसे काणठ स्पिरिट भी कहते है।
बनाने की विधि

गुणधर्म
- मेथेनाल एक रंगहीन द्रव है।
- इसका क्वथनांक 337.5K होता है।
- यह जल में घुलनशील है।
उपयोग –
- पेंट, वार्निश, सेल्यूलॉयड आदि में विलायक के रूप में ।
- फार्मेल्डिहाइड के निर्माण में ।
- एथेनाल के विकृतिकरण में।
- कार्बनिक यौगिक के निर्माण में ।
(2) ऐथेनॉल – रासायनिक सूत्र – C2H5OH
- यह मदिरा का मुख्य अंश है।
- इसे अन्न एल्कोहॉल भी कहते हैं।
- औद्योगिक रूप से ऐथेनॉल को शीरे या स्टार्चयुक्त पदार्थो के किण्वन द्वारा प्राप्त किया जाता है।

ऐथेनाल का उपयोग:-
- पेंट, वार्निश आदि में विलायक के रूप में ।
- पारदर्शी साबुन, रंग, पालिश, इत्र बनाने मे।
- औषधियो के निर्माण में।
फीनॉल [C6H5OH]
यह बेन्जीन का हाइड्राक्सी व्युत्पन्न है। इसमे एक या एक से अधिक – OH समूह ऐटोमैटिक वलय से सीधे जुड़े से रहते है।

फीनॉल बनाने की विधियां
(1) डाइएजोनियम लवणो के जल अपघटन द्वारा :-

(2) सल्फोनिक अम्ल से

(3) ग्रिगनाई अभिकर्मक से –

(4) बेंजीन के उत्प्रेरकी वायु ऑक्सीकरण से –

(5) हैलोबेंजीन के जल अपघटन से –

(6) क्यूमीन से –
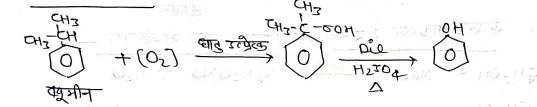
भौतिक गुणधर्म:-
- फीनाल रंगहीन व विशिष्ट गंध वाला ठोस पदार्थ है।
- फीनाल द्रव या निम्र गलनांक का ठोस होता है।
- यह ठण्डे जल मे कम विलेय ,जबकि कार्बनिक विलायको में पूर्ण विलेय होता है।
- (1v)अन्तराअणुक H- आबन्ध की उपस्थिति के कारण फीनॉल क्वथनांक उच्च होता है।
रासायनिक गुण
(1) प्रबल क्षारो से क्रिया:-

(2) सक्रिय धातु से क्रिया –

(3) ग्रिगनाई अभिकर्मक से क्रिया

(4) ऐसिटाइलीकरण –
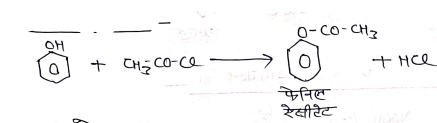
(5) Zn से अभिक्रिया

(6) एल्किलीकरण / ईथरीकरण/ विलियमसन संश्लेषण

(7) बेजाइलीकरण –
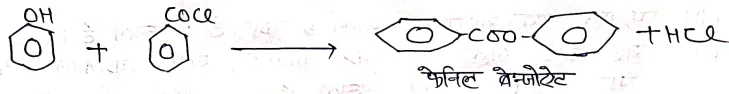
(8) PCl5 से क्रिया –

(9) हैलोजनीकरण

(10) नाइट्रीकरण –
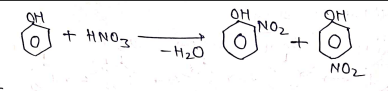
(11) NH3 से क्रिया –

(12) सल्फोनीकरण

(13) फ्रीडल क्रॉफ्ट एल्किलीकरण –

(14) फ्रीडल क्राफ्ट ऐसिलीकरण –

फीनॉल के उपयोग –
- बैकेलाइट, सैलिसिलिक अम्ल, एस्प्रिन के निर्माण में
- बिस तथा ऐजोरंजक के निर्माण में
फीनॉल का लीबरमान परीक्षण –
इस परीक्षण मे जब फीनॉल को सोडियम नाइट्राइट (NaNO2) तथा H2SO4 के मिश्रण के साथ गर्म किया जाता है तो एक विशिष्ट नींला या हरा रंग प्राप्त होता है। इस मिश्रण को जल के साथ तनु करने पर इनका रंग लाल हो जाता है तथा NaOH विलयन को आधिक्य मे मिलाने पर यह पुनः नीला हो जाता है
फीनॉल में अनुवाद

- अनुवाद के कारण फीनॉल अणु में ऑक्सीसीजन परमाणु पर e– घनत्व की कमी हो जाती है। जिसस O-H आबन्ध के e– ऑक्सीजन की ओर विस्थापित हो जाते है। फलस्वरूप हाइड्रोजन परमाणु प्रोटान मे परिवर्तित होने की प्रवृत्ति अर्जित कर लेता है तथा फीनॉल अम्लीय व्यवहार दर्शाने लगता है।
- एल्कोहॉल की अपेक्षा फीनॉल की अम्ल प्रबलता अधिक होती है।
- अम्ल प्रबलता का क्रम = CH3COOH> C6H5OH> C2H5OH
ईथर
- ईथर का क्रियात्मक समूह – 0- है।
- इनका सामान्य सूत्र CnH2n+2O
- ईथर एल्कोहॉल का एनहाइड्रारत है। 2ROH → ROR+H2O
- ईथर ऐल्कोहॉल के क्रियात्मक समावयव है।
- जब क्रियात्मक समूह (-O-) दो समान ऐल्किल समूह से जुड़ा होता है तो उन्हे सामान्य ईथर कहते हैं। जैसे – CH3-O-CH3, C2H5-O- C2H5
- जब क्रियात्मक समूह (-O-) दो भिन्न-भिन्न ऐल्किल समूह से जुड़ा होता है तो इसे मिश्रित ईथर कहते है| जैसे – CH3-O-CH2 CH3 , CH3-CH2-O-CH2-CH2-CH3
- ईथर में बन्ध कोण 110o होता है
- इनका साधारण नाम डाई एल्किल ईथर एवं एल्किल ,एल्किल ईथर (मिश्रित ईथर) से दिया जाता है।
ईथर के निर्माण की विधियां:-
1) विलयमसन ईथर संश्लेषण विधि:- इस विधि में सोडियम या पोटैशियम ऐल्कोक्साइड को ऐल्किल हैलाइड के साथ गर्म करने पर ईथर प्राप्त होता है। इस विधि द्वारा सरल और मिश्रित दोनो प्रकार के ईथर बनाये जा सकते हैं। इसे विलयमसन ईथर संश्लेषण कहते है।

(2) Rx को शुष्क Ag2O के साथ गर्म करके
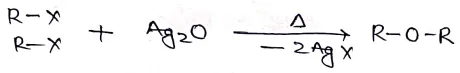
(3) प्रयोगशाला विधि:- प्रयोगशाला में डाई ऐथिल ईथर , ऐथिल एल्कोहॉल के आधिक्य और सान्द्र H2SO4 को 140°C पर गर्म करके बनाया जाता है।

ईथर के भौतिक गुण:-
- निम्न ईथर रंगहीन गैस या द्रव होते हैं।
- इनके क्वथनांक एल्कोहॉल से कम होते हैं क्योंकि इनमे H-bond नही बनते हैं।
- जल में कम घुलनशील व कार्बनिक विलायको मे अधिक घुलनशील होते हैं।
- ये जल से हल्के होते है अर्थात इनका घनत्व 1से कम होता है।
रासायनिक गुणधर्म –
(1) जल अपघटन:-

(2) PCl5 से क्रिया –

(3) ऐसीटिल क्लोराइड से क्रिया-

(4) कार्बन मोनो आक्साइड से क्रिया –

(5) अपचयन –

(6) ऐसीटिक ऐनहाइड्राइड से क्रिया:-

(7) दहन –

(9) ऑक्सीकरण –

(10) HI से क्रिया-

(11) हैलोजनीकरण-

(12) ऑक्सोनियम लवण बनना:- ठण्डे व सान्द्र H2SO4 अथवा HCl से अभिक्रिया करके यह ऑक्सोनियम लवण बनाता है।

(13) तप्त ऐलुमिना का प्रभाव-

उपयोग –
- प्रशीतक के रूप में।
- निश्चेतक के रूप में
- कार्बनिक विलायको के रूप में ।
- कृत्रिम सुगन्ध बनाने में।
Chapter 6 – हैलोएल्केन और हैलोएरीन नोट्स
Chapter 8 – ऐल्डिहाइड, किटोन एवं कार्बोक्सिलिक अम्ल नोट्स
Tagged with: Alcohols Phenols and Ethers notes in hindi | Chemistry chapter 7 class 12 notes in hindi | Chemistry class 12 chapter 7 in hindi notes | Chemistry class 12 chapter 7 notes in hindi | class 12 Chemistry chapter 7 ncert notes in hindi | Class 12 Chemistry Chapter 7 Notes in Hindi

thank you so much 👍 😊
ye download nhi ho raha hai
Niche me PDF Download ka button hai. Aap us pr click kr download kr lo
dil se thank you so much for this